1. 학습 목표
TLR4를 중심으로 그람음성 박테리아의 LPS를 감지하고, NFκB 및 IRAK4와 상호작용하여 세포내 염증 및 면역 반응을 활성화시키는 과정을 이해해 봅시다.
2. 핵심 내용
- TLR4를 통해 그람음성 박테리아에 감염된 대식세포는 LPS를 감지하고, NFκB를 활성화시켜 염증 싸이토카인을 분비하여 면역 반응을 촉진합니다.
- IRAK4 결핍 환자는 NFκB 부족으로 피막성 박테리아에 민감하나, TLR3와 TLR4는 바이러스 감염에 대응하여 일반적인 바이러스 감염에는 강한 면역 반응을 보입니다.
- TLR4의 신호 전달 경로는 MyD88, IRAK4, TRAF6 등이 연관되어 있어 염증 싸이토카인 생성과 NFκB 활성화를 중재함.
- TLR4는 두 번째 신호 전달 경로를 통해 바이러스 감염에 대한 인터페론 생성을 유도하여 항바이러스 면역 반응을 강화합니다.
3. 본문 내용
“Toll 유사 수용체를 통한 신호전달은 두 가지 싸이토카인 반응을 유도한다.”
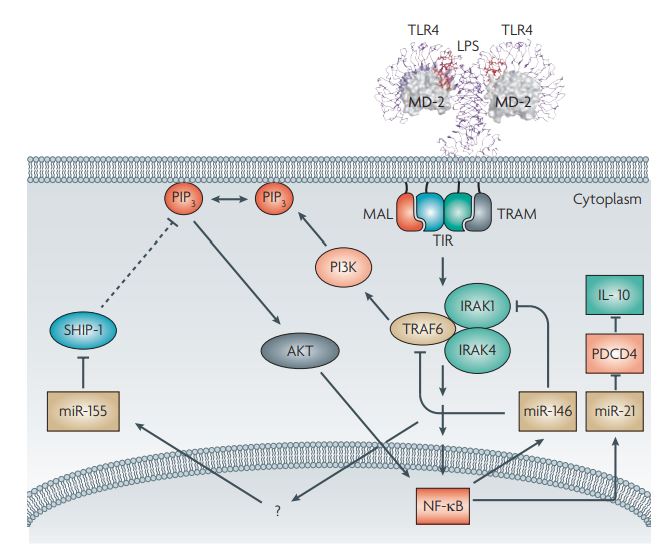
그람음성 박테리아에 감염된 조직에 있는 대식세포는 세포 표면의 TLR4, MD2, 그리고 CD14 복합체를 통해 세포외 LPS를 감지합니다. 이후, 대식세포는 염증 싸이토카인을 분비하도록 유도하는 세포 내 반응을 촉발합니다. 이 경로의 초기 부분은 세포질에서 일어나며, 전사인자 κB 핵인자(NFκB)의 활성을 유도합니다.
NFκB는 내재면역과 적응면역에서 모두 주요 역할을 하는 전사 인자로, 필요하지 않을 때는 κB 억제자(IκB)와 불활성 복합체를 형성하여 세포질 내에 유지됩니다. NFκB가 활성화되려면 이 복합체에서 분리되어 핵으로 이동해야 합니다. 핵 내에서 NFκB는 염증 싸이토카인 유전자의 전사를 개시하여 염증 반응을 촉진합니다. 이러한 과정은 감염 부위에서 염증을 유발하고, 동시에 감염을 제한하기 위한 중요한 면역 반응의 일부입니다.
TLR4 신호전달의 이동경로는 다음과 같습니다. 세포 외부에서 LPS가 인지되면 세포 내부에 있는 TLR4의 TIR 도메인이 MyD88 단백질 유사 TIR 도메인에 결합되도록 합니다. MyD88은 연결단백질(adaptor)의 예로 다른 신호전달 단백질 사이를 연결하는 다리의 역할을 합니다. 이들은 TIR 도메인과 죽음 도메인으로 알려진 유형의 두번째 도메인을 연결하는 방법으로 경로의 다음 구성원의 단백질키나아제 IRAK4를 끌어옵니다. 죽음 도메인은 세포가 잔해물을 남기지 않고 면역계를 자극하지 않는 정돈된 방법으로 죽는 정상적 과정인 세포자멸사(apoptosis)에 관여하는 단백질로 처음 발견되었기 때문에 이런 이름이 붙여졌습니다.
TLR4 신호전달의 이동경로는 다음과 같습니다. 세포 외부에서 LPS가 감지되면, 세포 내부에 있는 TLR4의 TIR 도메인이 MyD88(Myeloid differentiation primary response 88) 단백질의 TIR 도메인에 결합되도록 합니다. MyD88은 연결 단백질(adaptor protein)로, 다른 신호전달 단백질 사이를 연결하는 역할을 하는데, 이는 다음 단계의 신호 전달을 중재합니다. 이들은 TIR 도메인과 죽음 도메인으로 알려진 유형의 두 번째 도메인을 연결하는 방법으로 경로의 다음 구성원으로 IRAK4(Interleukin-1 receptor-associated kinase 4)를 끌어옵니다. 죽음 도메인은 세포자멸사(apoptosis)에 관여하는 단백질로서, 세포가 정상적인 과정으로 정돈된 방식으로 죽을 때 면역계를 자극하지 않고 잔해물을 남기지 않는 역할을 합니다. 이 도메인의 이름은 처음에 이 단백질이 세포자멸사와 관련이 있어 발견됐기 때문에 붙여진 것입니다. 이러한 신호전달 경로를 통해 TLR4는 세포 내에서 염증 싸이토카인 유전자의 활성화를 촉진하고, 결과적으로 염증 반응을 유발합니다.
단백질 키나아제는 다른 단백질에 인산을 추가하는 효소로, 이 인산화는 표적 단백질의 활성을 변화시키거나 특정 단백질과의 상호작용을 가능하게 합니다. 따라서 단백질 키나아제는 세포 내 신호전달 경로의 핵심 구성 성분 중 하나입니다. IRAK4는 죽음 도메인을 가지고 있어 MyD88의 죽음 도메인과 결합합니다. 이 결합은 단백질 키나아제를 활성화시키고, 자체를 인산화시키며, 이로써 복합체에서 떨어져 나와 TRAF6(특정 단백질과 상호작용하는 연결 단백질)를 인산화시킵니다. 경로상의 몇 단계를 더 거치면 최종적으로 κB 키나아제 억제자(IKK)라는 키나아제 복합체의 활성을 유도합니다. 이 억제자가 방출되면, κB 키나아제 억제자(IKK)는 핵으로 이동하여 거기서 대식세포의 효과 기능을 확대하고, 강도를 증가시키는 싸이토카인, 부착 분자, 그리고 다른 단백질의 활성을 유도합니다. 이는 염증 반응을 촉진하고, 감염 부위의 면역 활동을 강화하는 과정 중 하나입니다.
대부분의 Toll 유사 수용체는 MyD88 연결단백질을 통해 IKKγ를 활성화시키는 경로를 통해 주로 신호를 전달합니다. 그러나 TLR3은 이와는 별도로, 인터페론 반응인자 3(IRF3)의 활성을 유도하는 두 번째 신호전달 경로를 통해 I형 인터페론을 생성합니다. 이는 항바이러스 싸이토카인의 생산을 유발합니다. TLR4도 이러한 두 번째 경로를 활용하며, 이는 사람 Toll 유사 수용체 중에서 유일하게 두 경로를 모두 활용하는 경우입니다. 두 번째 경로에서는 MyD88이 아닌 Toll 수용체 연관 인터페론 활성자(TRIF)와 Toll 수용체 연관 분자(TRAM)라는 두 개의 다른 연결단백질이 관여합니다. 이러한 연결단백질은 리간드를 감지한 후 TLR3 또는 TLR4와 복합체를 형성하고, TRAF6와 관련된 TRAF3이 참여하는 신호전달 경로를 개시하여 세포질에 있는 IRF3의 인산화를 유도하는 인산화 효소 연쇄 경로를 시작합니다. 인산화된 IRF3는 핵으로 들어가서 바이러스 및 세포내 박테리아 감염에 대한 내재면역반응의 핵심인 I형 인터페론 및 싸이토카인 유전자의 전사를 주도합니다. 이는 감염에 대한 면역반응을 강화하는 중요한 과정 중 하나입니다.
이 신호 전달 경로는 현재까지 가장 잘 연구된 TLR(Toll-Like Receptor)에 의해 활성화되는 경로 중 하나입니다. 이는 TLR을 가진 대식세포와 다른 세포가 다양한 유형의 감염에 대한 내재면역 반응을 어떻게 조절하는지 설명합니다. 세포외 박테리아 감염에 대해선 염증 싸이토카인을 생산하여 감염을 효과적으로 제거할 수 있지만, 바이러스 감염에 대해서는 바이러스를 더 효과적으로 제거할 수 있는 인터페론을 생산합니다. 이 구분은 IRAK4 키나아제 결핍 환자가 질병에 민감하게 반응하는 이유를 설명할 수 있습니다. 이 환자들은 NFκB를 효과적으로 활성화시키지 못하므로 염증 싸이토카인의 생산 능력이 감소하게 되어 피막성 박테리아의 반복 감염에 취약해집니다. 그러나 동시에, 이들은 TLR3와 TLR4의 능력이 정상이기 때문에 대부분의 일반적인 바이러스 감염에 대해 효과적으로 대응할 수 있습니다.
4. 정리
그람음성 박테리아에 감염된 조직에서 대식세포가 TLR4를 통해 염증 싸이토카인을 분비하고 NFκB 신호를 활성화 시킨다.
대식세포의 역할: 그람음성 박테리아에 감염된 조직의 대식세포는 세포 표면의 TLR4, MD2, 그리고 CD14 복합체를 통해 세포외 LPS를 감지합니다.
NFκB의 역할: 대식세포 내에서 TLR4의 활성화는 세포질에서 일어나며, NFκB의 활성을 유도합니다. NFκB는 염증 싸이토카인 유전자의 전사를 개시하여 염증 반응을 촉진합니다.
NFκB의 활성화 경로: TLR4 신호전달의 이동경로는 MyD88 단백질과 IRAK4를 포함하는 경로를 따르며, 이는 NFκB의 활성화를 유도합니다. 죽음 도메인이 관여하여 죽음 도메인을 가진 다른 단백질들과 상호작용합니다.
키나아제와 NFκB의 활성화: 이 신호전달 경로에서는 단백질 키나아제가 다양한 중간체에 작용하여 NFκB의 활성화를 유도하고, 염증 반응을 촉진합니다.
TLR4의 두 가지 신호전달 경로: TLR4는 MyD88에 의한 경로뿐만 아니라, TRIF와 TRAM에 의한 두 번째 신호전달 경로를 통해도 활성화됩니다. 이는 I형 인터페론의 생성을 유도하여 바이러스 감염에 대한 내재면역 반응을 촉진합니다.
IRAK4의 역할: IRAK4는 MyD88과 죽음 도메인을 통해 TLR4의 TIR 도메인과 상호작용하여 단백질 키나아제의 활성화를 유도합니다.
TLR4의 복합체 형성: TLR4는 LPS를 감지하면 MyD88, IRAK4, TRIF, TRAM 등과 상호작용하여 복합체를 형성하고, 이를 통해 다양한 신호전달 경로를 개시합니다.
IRF3의 인산화와 인터페론 생성: TLR4의 두 번째 신호전달 경로에서는 TRIF와 TRAM을 통해 IRF3의 활성화와 인산화가 유도되어 바이러스 감염에 대한 I형 인터페론의 생성이 촉진됩니다.
IRAK4 키나아제 결핍 환자의 취약성: IRAK4 키나아제 결핍 환자는 NFκB를 효과적으로 활성화시키지 못해 염증 싸이토카인의 생산 능력이 감소하므로, 특히 피막성 박테리아의 감염에 민감하게 반응합니다. 그러나 TLR3와 TLR4의 능력이 정상이기 때문에 바이러스 감염에 대해서는 효과적으로 대응할 수 있습니다.
참고문헌- 면역학 3판, 라이프사이언스
'면역학' 카테고리의 다른 글
| [내재면역] "면역 전문 살해자, 호중구: 감염 부위로의 민첩한 침투와 활약" (2) | 2024.01.16 |
|---|---|
| [내재면역] "Toll 유사 수용체의 비밀: 면역의 실제 전술과 생체반응 해부" (0) | 2024.01.16 |
| "면역의 감시탑: Toll 유사 수용체의 다양한 미생물 감지와 면역조절" (0) | 2024.01.16 |
| 미생물과의 상호작용, 대식세포의 수용체와 내재면역의 효과적인 대응 (0) | 2024.01.15 |
| 보체 활성화와 면역 체계의 공동 작용, 염증 유도 및 감염 대응 메커니즘 (2) | 2024.01.13 |



